
Mục lục
Tế bào gốc trung mô (MSC) được xem là một ứng cử viên hàng đầu cho các liệu pháp dựa trên tế bào. Chúng sở hữu tính đa năng, với tiềm năng biệt hóa thành xương, sụn, mỡ và khả năng điều hòa miễn dịch bằng việc ức chế phản ứng viêm và giải phóng các yếu tố kích thích sửa chữa mô.
Phương pháp sử dụng trực tiếp MSC điều trị trong lâm sàng đối mặt với một số rủi ro. Trong đó, truyền tĩnh mạch sẽ liên quan đến độc tính khi truyền. Sự hình thành mô lạc chỗ và quá trình hình thành khối u cũng là mối quan tâm nếu sự tăng sinh và biệt hóa trở nên mất kiểm soát.
Là một phương pháp tiếp cận thay thế, việc sử dụng các túi ngoại bào (EV) có nguồn gốc từ MSC đang ngày càng được chú ý. MSC giải phóng các EV như exosome và microvesicle, làm trung gian cho sự giao tiếp giữa các tế bào và phản ánh nhiều tác dụng điều trị của chính MSC. So với các phương pháp điều trị dựa trên tế bào, EV có thể là một mô hình khả thi và thực tế hơn.
Extracellular vesicles (EV) là gì?
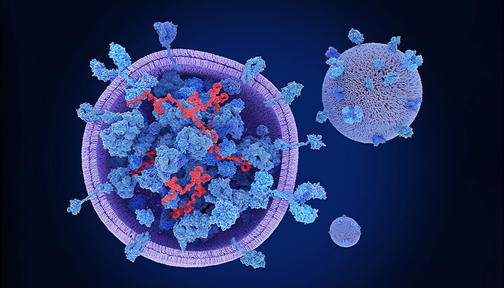
Các túi ngoại bào (EV) là một quần thể không đồng nhất, được bao bọc bởi một lớp kép lipid với các kích thước, quá trình sinh tổng hợp, thành phần và chức năng khác nhau. Chúng được tiết ra từ hầu hết các loại tế bào trong cơ thể và chứa các thành phần của tế bào cho, bao gồm nhiều loại protein, lipid và phân tử axit nucleic cụ thể. Do đó, ở một mức độ nhất định, chúng thừa hưởng các đặc tính chức năng của tế bào mẹ và được coi là thành phần quan trọng trong giao tiếp giữa các tế bào, góp phần chữa lành các mô và cơ quan bị thương hoặc bị bệnh. Exosome vận chuyển các hàng hóa chức năng như các phân tử miRNA và mRNA, peptide, protein, cytokine và lipid từ MSC đến các tế bào nhận.
Theo đường kính hoặc quá trình sinh tổng hợp, EV thường được chia thành ba phân nhóm chính, tức là exosome, microvesicle và thể apoptosis. Microvesicle và thể apoptosis (kích thước lớn hơn 100 nm) là các túi có nguồn gốc từ sự nảy chồi và tách ra khỏi bề mặt màng plasma, trong khi exosome (đường kính 30–150 nm) là các túi có nguồn gốc từ nội bào.
Việc ứng dụng exosome làm chất sinh học điều trị có nhiều lợi thế hơn so với sử dụng MSC trực tiếp.
Đầu tiên, exosome có thể được lưu trữ và vận chuyển ở nhiệt độ thấp trong thời gian dài hơn mà không bị mất đáng kể hoạt tính sinh học so với tế bào. Thứ hai, exosome có khả năng thẩm thấu tốt hơn để vượt qua các hàng rào sinh học, chẳng hạn như hàng rào máu não và tránh bị mắc kẹt trong các cơ quan hoặc mô. Ngoài ra, màng kép lipid của chúng có thể bảo vệ hoạt tính sinh học của các phân tử bên trong trong môi trường sinh lý phức tạp. Thứ ba, exosome có thể được thiết kế với các đặc tính cụ thể và truyền vào cơ thể bệnh nhân với số lượng lớn để có được hiệu quả lâm sàng tốt hơn. Cuối cùng, chúng an toàn hơn liệu pháp cấy ghép tế bào, với ít nguy cơ chuyển đổi thành khối u và kích hoạt phản ứng miễn dịch.
Những cân nhắc chính trong ứng dụng của Exosome
Khi xem exosome như tác nhân sinh học trong ứng dụng lâm sàng, có một loạt các thách thức không thể bỏ qua ở các khía cạnh kiểm soát chất lượng và quy định trong sản xuất exosome. Do thiếu các tiêu chuẩn hóa trong phương pháp luận hoặc quy trình thu thập và phân lập exosome, các sản phẩm exosome thường khác nhau về tính an toàn và chất lượng. Do đó, việc sản xuất exosome phải tuân theo các quy trình thực hành sản xuất tốt giống như các chế phẩm dược phẩm khác để đáp ứng mức độ an toàn cấp độ lâm sàng. Môi trường không chứa huyết thanh động vật được khuyến nghị dùng trong nuôi cấy MSC để tránh trộn lẫn các exosome ngoại sinh có nguồn gốc từ huyết thanh động vật. Ngoài ra, công nghệ kỹ thuật sinh học có thể được áp dụng để sửa đổi kiểu hình hoặc thành phần của exosome, có thể thêm hoặc bớt các phân tử sinh học cụ thể trong exosome để tăng hiệu quả hoặc giảm các tác dụng không mong muốn trong quá trình điều trị.
Tính đồng nhất và kiểm soát chất lượng cũng là những cân nhắc hoặc thách thức quan trọng trong khía cạnh quản lý. Tính đồng nhất của exosome không thể đạt được một cách chắc chắn vì với các loại thuốc được xác định về mặt hóa học, ngay cả các exosome từ cùng một tế bào cũng không đồng nhất. Việc phát triển phương pháp sàng lọc exosome bằng các marker bề mặt được xem là một phương pháp để thu nhận các exosome đồng nhất hơn. Mặc dù việc thiếu chuẩn hóa trong phương pháp thu thập, phân lập và phân tích exosome có thể ảnh hưởng đến hàm lượng và hiệu lực của exosome, chúng ta vẫn có thể xác định hàm lượng hoạt động chính chịu trách nhiệm cho hiệu quả điều trị bằng xét nghiệm bất hoạt. Ngoài ra, sau khi xác định được hàm lượng hoạt động, chúng ta có thể sử dụng chúng để thiết lập kiểm soát chất lượng như mô tả ở trên và xác định phương pháp tốt nhất để thu thập, phân lập và tinh chế exosome.
Quý khách hàng có thể tham khảo các sản phẩm về exosome mà Biogroup cung cấp tại đây.
Tài liệu tham khảo
Hu JC, Zheng CX, Sui BD, Liu WJ, Jin Y. Mesenchymal stem cell-derived exosomes: A novel and potential remedy for cutaneous wound healing and regeneration. World J Stem Cells. 2022 May 26;14(5):318-329. doi: 10.4252/wjsc.v14.i5.318. PMID: 35722196; PMCID: PMC9157601.
Roszkowski S. Therapeutic potential of mesenchymal stem cell-derived exosomes for regenerative medicine applications. Clin Exp Med. 2024 Mar 1;24(1):46. doi: 10.1007/s10238-023-01282-z. PMID: 38427086; PMCID: PMC10907468.