Tinh sạch EV: Ảnh hưởng của môi trường nuôi cấy đến hiệu suất thu hồi EV
Trong sản xuất Túi ngoại bào (EVs), dịch nổi tế bào (Conditioned Media – CM) là nguồn nguyên liệu chính. Tuy nhiên, thực tế tại nhiều đơn vị cho thấy, dù tế bào MSC tăng sinh rất tốt, nhưng khi bước vào giai đoạn tinh sạch, các nhóm nghiên cứu thường rơi vào hai trường hợp sau:
Tắc nghẽn trong quá trình lọc: Môi trường quá nhớt khiến ngay cả bước lọc thô 0.45 um để loại bỏ mảnh vỡ tế bào cũng trở nên khó khăn. Có khách hàng chạy siêu ly tâm (UC) ở quy mô nhỏ thì kết quả rất ổn định. Nhưng khi chuyển sang các hệ thống lọc màng để mở rộng quy mô thì lọc bị nghẹt liên tục, sản lượng EV thu được thấp hơn hẳn quy trình truyền thống. Họ bị kẹt lại với phương pháp UC thủ công, không thể tiến lên quy mô sản xuất công nghiệp vì nỗi lo thất thoát mẫu trên màng lọc.
Số hạt thu được tăng nhưng hoạt tính giảm: Tổng số hạt đo được sau tinh sạch tăng rất cao, nhưng khi sử dụng cùng một liều lượng hạt (hạt/mL) cho các phân tích chức năng, hoạt tính sinh học lại giảm xuống.
Mục lục
ToggleQuan hệ mật thiết giữa quy trình nuôi cấy upstream và tinh sạch downstream
Vậy tại sao lại có sự khác biệt như phần trên? Câu trả lời nằm ở mối quan hệ mật thiết giữa quy trình nuôi cấy upstream và tinh sạch downstream. Trong sản xuất EVs, môi trường nuôi cấy không chỉ đóng vai trò nuôi tế bào, kích thích sản xuất EVs, mà còn quyết định sự thông suốt của toàn bộ hệ thống xử lý hạ nguồn.
Hiểu rõ những điểm nghẽn này, chúng tôi mang đến một giải pháp toàn diện gồm môi trường sản xuất EVs chuyên dụng CellCorTM EXO CD và máy tinh sạch EV tự động EXODUS, giúp quy trình sản xuất EV không chỉ dừng lại ở quy mô lab nghiên cứu mà có thể mở rộng quy mô lên sản xuất công nghiệp đáp ứng được các quy định của GMP.
Quy trình tinh sạch EV
Quy trình sản xuất EVs tiêu chuẩn thường được triển khai qua 4 giai đoạn chính:
- Rã đông và tăng sinh tế bào gốc trung mô người (MSC) trong môi trường nuôi cấy chuyên dụng.
- Chuyển đổi từ môi trường tăng sinh sang môi trường sản xuất EVs (như CellCor™ EXO CD) để thu nhận dịch nổi (Conditioned Media – CM).
- Phân lập và tinh sạch EVs. Đây là bước quan trọng nhằm loại bỏ tạp chất, protein tự do và nucleic acid nội sinh hoặc từ môi trường.
- Thu nhận EVs tinh khiết, pha chế, phối trộn và hoàn thiện sản phẩm cuối cùng.

Khác với quy trình thu hoạch tế bào thông thường, việc phân lập EVs đối mặt với những thách thức kỹ thuật phức tạp hơn, đặc biệt là khi mở rộng quy mô. Hiện nay, các phương pháp như siêu ly tâm (UC) (1), siêu ly tâm tỷ trọng (Density-gradient UC) (2), sắc ký lọc gel (SEC), siêu lọc (ultrafiltration) (3) hoặc quy trình kết hợp của những phương pháp trên vẫn được dùng trong nghiên cứu nhưng lại bộc lộ hạn chế khi sản xuất công nghiệp (4).
Đối với quy mô sản xuất lớn (từ 1–10L hoặc hơn), các công nghệ dựa trên màng lọc là lựa chọn tối ưu nhờ khả năng nâng cấp quy mô linh hoạt:
- Hệ thống EXODUS: Giải pháp đột phá với khả năng tự động hóa hoàn toàn, loại bỏ sai sót do thao tác thủ công, đảm bảo tính đồng nhất tuyệt đối giữa các mẻ sản xuất. EXODUS không chỉ tối ưu hiệu suất thu hồi mà còn tích hợp các tính năng truy xuất nguồn gốc dữ liệu (audit trail) và nhật ký thời gian thực (timestamp log). Đây là những yếu tố then chốt đảm bảo tính toàn vẹn dữ liệu, đáp ứng nghiêm ngặt tiêu chuẩn GMP trong sản xuất dược phẩm sinh học (5).
- Hệ thống lọc tiếp tuyến (TFF – Tangential Flow Filtration): Cho phép xử lý thể tích mẫu lớn, có khả năng nâng cấp quy mô tốt. Khi được tích hợp vào các hệ thống chạy tự động, TFF có khả năng ghi lại dữ liệu vận hành theo từng lô (batch), hỗ trợ đáp ứng các yêu cầu về hồ sơ GMP.
Mặc dù các hệ thống tinh sạch EV hiện đại là lời giải cho bài toán sản xuất EV ở quy mô công nghiệp, nhưng hiệu suất tinh sạch của hệ thống này vẫn phụ thuộc lớn vào chất lượng dịch nổi nuôi cấy tế bào đầu vào. Nếu quy trình nuôi cấy không được tối ưu, quá trình xử lý hạ nguồn sẽ phải đối mặt với những vấn đề làm đội chi phí sản xuất và giảm hiệu suất thu hồi.
Vấn đề 1: Ảnh hưởng của thành phần dịch nổi tế bào đến hiệu suất tinh sạch EV
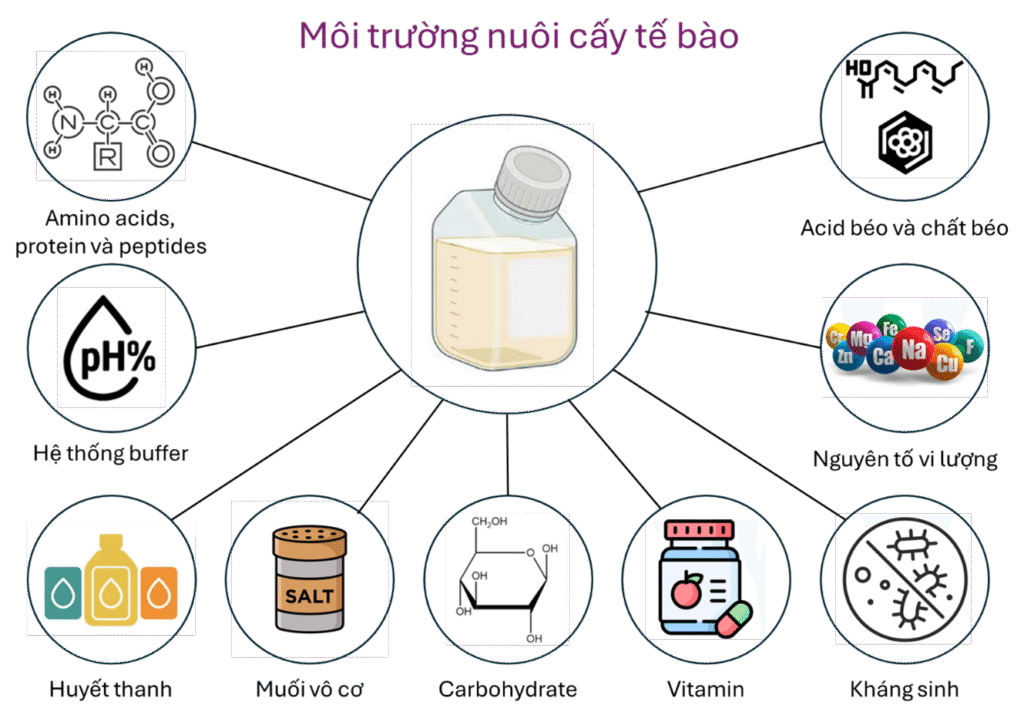
Trong thực tế vận hành, dịch nổi sau quá trình nuôi cấy MSC không còn là dung dịch trong suốt đơn thuần. Nó trở thành một hỗn hợp phức tạp với độ nhớt tăng, chứa đựng những thành phần không thấy được bằng mắt thường, nhưng có ảnh hưởng đến quá trình lọc hạ nguồn:
- Protein bám dính và sợi ngoại bào: MSC trong quá trình tăng sinh có thể tiết ra collagen, fibronectin, filamin và các protein cấu trúc nên chất nền ngoại bào (6,7). Những đại phân tử này có khối lượng phân tử lớn, có khả năng tạo thành một mạng lưới bao quanh tế bào và EVs, làm tăng đáng kể độ nhớt của dịch nổi.
- RNA tự do (non-vesicular RNA): Tồn tại trong môi trường sau quá trình nuôi cấy (8). Những sợi RNA này có thể tương tác với protein trong môi trường nuôi cấy tạo thành phức hợp protrin-RNA, có thể bám vào màng lọc và bịt kín các lỗ lọc.
- Protein trong môi trường nuôi cấy: Nhiều môi trường nuôi cấy MSC hiện nay sử dụng Albumin (có nguồn gốc từ huyết thanh hoặc dạng tái tổ hợp). Đây là loại protein có tính bám dính cực mạnh trên các bề mặt kỵ nước (hydrophobic), đặc biệt không tương thích với các phương pháp lọc dưới áp suất cao, gây ra hiện tượng nghẹt màng nhanh chóng (9).
- Polymer và các chất không xác định khác: Các polymer được sử dụng để ổn định growth factor trong môi trường chemical defined (10), hoặc các thành phần không xác định trong huyết thanh (serum/hPL) (nếu môi trường nuôi MSC có sử dụng serum) có thể tạo nên một mạng lưới bao vây lỗ lọc, giảm tốc độ lọc.
Sự hiện diện của các nhân tố kể trên có thể dẫn đến hiện tượng nghẹt màng (fouling) trong quá trình tinh sạch EV hạ nguồn. Điều này tạo ra một hệ lụy cho quy trình sản xuất, làm tăng chi phí vật tư tiêu hao, tiêu tốn nguồn nhân lực để xử lý sự cố, đồng thời còn đối mặt với nguy cơ tạp nhiễm và rủi ro không thể lặp lại quy trình giữa các lô sản xuất, tạo thành một rào cản lớn đối với tiêu chuẩn GMP.
Nghiêm trọng hơn, chính đặc tính bám dính này khiến các hạt EV bị kéo theo hoặc cuộn chặt vào các phức hợp protein tạp, dẫn đến tình trạng thất thoát mẫu ngay trên màng lọc. Kết quả là hiệu suất thu hồi bị sụt giảm, khiến quy trình sản xuất trở nên tốn kém.
Dấu hiệu nhận biết sớm:
- Dịch nổi có độ nhớt cảm quan cao.
- Tốc độ dòng chảy sụt giảm nhanh chóng ngay từ bước tiền xử lý (Pre-filtration) qua các màng lọc 5 um, 0.45 um cho đến 0.22 um.
Vấn đề 2: Tạp nhiễm các hạt nhỏ vào quy trình tinh sạch và thành phẩm
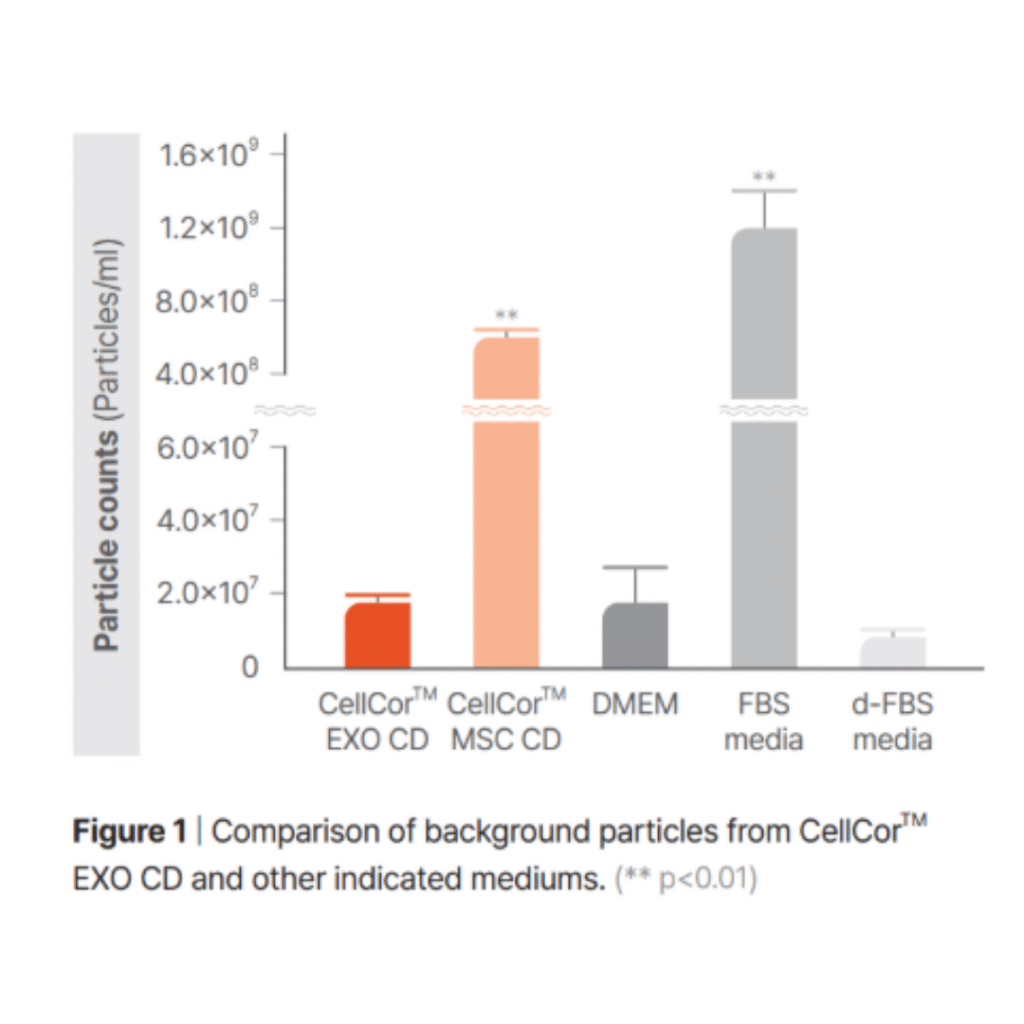
Trong các hệ thống phân lập EV dựa trên kích thước như EXODUS hoặc lọc màng tiếp tuyến (TFF), màng lọc sẽ giữ lại tất cả những gì nằm trong phạm vi kích thước mục tiêu. Tuy nhiên, những hạt có cùng kích thước nhưng không phải là EV cũng sẽ được giữ lại trong quá trình lọc và có thể xuất hiện trong sản phẩm EV cuối cùng.
Các nguồn tạp nhiễm hạt phổ biến:
- Hạt nội tại của môi trường: Nhiều dòng môi trường nuôi cấy MSC vẫn chứa các hạt nền được hình thành trong quá trình sản xuất.
- Huyết thanh bổ sung từ động vật/người: Huyết thanh bò (FBS) hay dịch ly giải tiểu cầu người (hPL) chứa một lượng rất cao những hạt ngoại lai (cả EV lẫn những hạt có kích thước giống EV như hạt lipoprotein) (11). Để loại bỏ những hạt này, huyết thanh cần được xử lý loại bỏ EV trước khi sử dụng. Tuy nhiên, khi loại bỏ EV, khả năng hỗ trợ tăng sinh của môi trường bị sụt giảm.
- Tương tác hóa lý từ các chất bổ sung: Các thành phần mà mỗi lab tự thêm vào môi trường nuôi cấy MSC có thể tương tác với nền môi trường, hình thành các hạt tụ (aggregates) có kích thước ngẫu nhiên nằm đúng vào kích thước của EV.
Đối với những môi trường nuôi cấy có nồng độ hạt nền cao, có nguy cơ những hạt nền này sẽ đi vào sản phẩm EV tinh sạch cuối cùng sau quá trình phân lập. Sự hiện diện của các hạt ngoại lai sẽ dẫn đến sự sai lệch trong việc đánh giá chất lượng sản phẩm cuối cùng.
Cụ thể, dù tỷ số hạt / µg protein có thể tăng cao, nhưng thực chất quần thể MSC-EVs mục tiêu lại bị sụt giảm do sự pha trộn của các hạt tạp ngoại lai. Việc xác định liều lượng (dosage) dựa trên tổng số hạt đo bằng NTA hoặc RPS lúc này sẽ dẫn đến nồng độ EV thực tế thấp hơn dự kiến. Sự sai lệch này không chỉ làm suy giảm hiệu năng của các thử nghiệm in vitro và in vivo, mà còn tiềm ẩn nguy cơ gây phản ứng miễn dịch không mong muốn.
Phương pháp phát hiện: Sử dụng các thiết bị đếm hạt nano chuyên dụng như phân tích truy vết hạt nano (NTA – Nanoparticle Tracking Analysis) hoặc cảm biến xung điện trở (RPS – Resistive Pulse Sensing). Các thiết bị này cho phép định lượng chính xác nồng độ hạt và phân tích phân bố kích thước của các hạt tồn tại sẵn trong môi trường nuôi cấy.
Giải pháp từ CellCor™ EXO CD: Tối ưu hóa cho quy trình tinh sạch EV hạ nguồn
Hiểu rõ những thách thức trong việc mở rộng quy mô sản xuất EV, môi trường CellCor™ EXO CD được thiết kế với triết lý tương thích với quy trình hạ nguồn:
- Độ tinh sạch cao: Với nồng độ hạt nền chỉ ở ngưỡng 2 x107 hạt/mL, CellCor™ EXO CD giảm thiểu tối đa rủi ro về sự tạp nhiễm của các hạt ngoại lai vào thành phẩm EVs.
- Giảm thiểu nền môi trường gây nghẹt: Công thức hóa học hoàn toàn xác định (chemically defined) giúp xác định và điều chỉnh hàm lượng những chất gây nghẹt màng ngay từ đầu. Điều này giúp bảo vệ màng lọc, duy trì tốc độ dòng chảy ổn định và giảm thiểu chi phí vận hành.
- Tăng sản lượng, giảm thất thoát: CellCor™ EXO CD được tối ưu để kích thích tế bào MSC giải phóng EV nhiều hơn, đồng thời được thiết kế để tương thích với hệ thống lọc EXODUS hoặc TFF.
TÀI LIỆU THAM KHẢO
1. Ramírez-Bajo MJ, Banon-Maneus E, Rovira J, Campistol JM, Diekmann F. Isolation of Extracellular Vesicles Derived from Mesenchymal Stromal Cells by Ultracentrifugation. Bio-Protoc. 2020 Dec 20;10(24):e3860.
2. Abyadeh M, Mirshahvaladi S, Kashani SA, Paulo JA, Amirkhani A, Mehryab F, et al. Proteomic profiling of mesenchymal stem cell-derived extracellular vesicles: Impact of isolation methods on protein cargo. J Extracell Biol. 2024;3(6):e159.
3. Karttunen J, Heiskanen M, Joki T, Hyysalo A, Navarro-Ferrandis V, Miettinen S, et al. Effect of cell culture media on extracellular vesicle secretion from mesenchymal stromal cells and neurons. Eur J Cell Biol. 2022;101(4):151270.
4. Liangsupree T, Multia E, Riekkola ML. Recent advances in modern extracellular vesicle isolation and separation techniques. J Chromatogr A. 2026 Jan 25;1767:466602.
5. Exodus T-2800 [Internet]. Exodus Bio. [cited 2026 Feb 4]. Available from: https://www.exodusbio.com/exodus-t-2800/
6. Chen X, Dusevich V, Feng JQ, Manolagas SC, Jilka RL. Extracellular Matrix Made by Bone Marrow Cells Facilitates Expansion of Marrow‐Derived Mesenchymal Progenitor Cells and Prevents Their Differentiation Into Osteoblasts*. J Bone Miner Res. 2007 Dec 1;22(12):1943–56.
7. Zeng X, Ma Y, Chen Y, Qiu X, Wu J, Ling E, et al. Autocrine fibronectin from differentiating mesenchymal stem cells induces the neurite elongation in vitro and promotes nerve fiber regeneration in transected spinal cord injury. J Biomed Mater Res A. 2016 Aug;104(8):1902–11.
8. Corso G, Mäger I, Lee Y, Görgens A, Bultema J, Giebel B, et al. Reproducible and scalable purification of extracellular vesicles using combined bind-elute and size exclusion chromatography. Sci Rep. 2017 Sep 14;7:11561.
9. Cirillo AI, Tomaiuolo G, Guido S. Microfiltration of concentrated albumin solutions and the role of processing conditions on membrane fouling. Chem Eng J Adv. 2023 Nov 15;16:100561.
10. Masuzawa Y, Kitazawa M. Synthetic polymers as xeno-free materials for stabilizing basic fibroblast growth factor in human mesenchymal stem cell cultures. Biochem Biophys Rep. 2021 Mar 1;25:100929.
11. Khmelnytska YM, Pykhtieiev DM, Yuriev BV, Svoboda MF, Gumeniuk MI. Comparison of EV isolation methods from MSCs. Biopolym Cell. 2025;41(3):200.
Danh mục
- Blog (67)
- Tin tức (44)
- Tuyển dụng (11)
- Sản Phẩm & Công Nghệ Mới (50)
- Đào Tạo & Webinar (24)
- Gian Hàng Ảo (1)